কিভাবে একটি রসায়ন পরীক্ষা পাস করতে হবে
লেখক:
Roger Morrison
সৃষ্টির তারিখ:
3 সেপ্টেম্বর 2021
আপডেটের তারিখ:
1 জুলাই 2024

কন্টেন্ট
- পর্যায়ে
- পার্ট 1 ভাল অধ্যয়নের অভ্যাস বিকাশ
- পার্ট 2 পারমাণবিক কাঠামো বোঝা
- পার্ট 3 রাসায়নিক প্রতিক্রিয়ার পূর্বাভাস
- অংশ 4 রসায়নে গণিত প্রয়োগ করা
- পর্ব 5 রসায়নের ভাষা ব্যবহার করে
একটি সাধারণ রসায়ন কোর্সে সাফল্য অর্জন করতে আপনাকে অবশ্যই এই বিষয়টির মৌলিক বিষয়গুলি বুঝতে হবে, সাধারণ গণনা করতে সক্ষম হতে হবে, আরও জটিল ক্রিয়াকলাপ সম্পাদনের জন্য একটি ক্যালকুলেটর ব্যবহার করতে হবে এবং সত্যিই আলাদা কিছু শেখার জন্য প্রস্তুত থাকতে হবে। রসায়ন এমন একটি বিজ্ঞান যা পদার্থ এবং এর বৈশিষ্ট্যগুলি অধ্যয়ন করে। আমাদের চারপাশের সমস্ত কিছু রসায়ন সম্পর্কিত, এমনকি আপনি যে প্রাকৃতিক পানীয় হিসাবে পান করেন এবং বায়ু বৈশিষ্ট্য যা আপনি শ্বাস প্রশ্বাস গ্রহণ করেন সেগুলির মতো প্রাথমিক বিষয়গুলিও আপনি একেবারে প্রাকৃতিক বিবেচনা করতে পারেন। পারমাণবিক স্তরে এমনকি আপনার চারপাশের বিশ্বকে বোঝার ক্ষেত্রে নতুন জ্ঞানের জন্য উন্মুক্ত থাকুন। রসায়নের সাথে আপনার প্রথম যোগাযোগ চ্যালেঞ্জিং এবং উত্তেজনাপূর্ণ হতে পারে।
পর্যায়ে
পার্ট 1 ভাল অধ্যয়নের অভ্যাস বিকাশ
-

আপনার শিক্ষককে জানতে শিখুন। রসায়ন ক্লাসে সাফল্য পেতে এবং ক্লাসে আরও ভাল গ্রেড পাওয়ার জন্য, আপনার শিক্ষকের সাথে দেখা করার জন্য সময় নিন এবং যা আপনি বুঝতে পারছেন না তার সাথে ভাগ করুন।- অনেক শিক্ষকের অধ্যয়নের গাইড রয়েছে এবং প্রয়োজনের সময় স্কুল সময়ের বাইরে শিক্ষার্থীদের গ্রহণ করতে ইচ্ছুক।
-

গঠন বা একটি অধ্যয়ন গ্রুপ যোগদান। রসায়ন কোর্সগুলি বেশ জটিল দেখলে লজ্জা পাবেন না। এটি প্রায় প্রত্যেকের পক্ষে একটি কঠিন বিষয়।- আপনি যদি একটি দলে যোগদান করেন তবে কিছু সদস্য কোর্সের কিছু অংশ অন্যদের চেয়ে সহজতর খুঁজে পেতে পারেন এবং তাদের শিক্ষার পদ্ধতিগুলি সবার সাথে ভাগ করে নিতে পারেন। কাজগুলি ভাগ করুন।
-

অধ্যায় পড়ুন। রসায়ন পাঠ্যপুস্তক সবসময় পড়া সবচেয়ে আকর্ষণীয় বই হয় না। তবুও, আপনাকে দেওয়া ক্লাসিকগুলি পড়ার জন্য আপনাকে অবশ্যই সময় নিতে হবে এবং যে অংশগুলি আপনি বুঝতে পারছেন তা হাইলাইট করুন। আপনি বুঝতে না পারছেন এমন প্রশ্ন বা ধারণাগুলির একটি তালিকা তৈরি করার চেষ্টা করুন।- এই হার্ড-টু বোঝার অংশগুলি আবার পড়ার চেষ্টা করুন। আপনি যদি এখনও সেগুলি বুঝতে না পারেন তবে তাদের আপনার অধ্যয়ন দল, আপনার শিক্ষক বা আপনার সহকারী অধ্যাপকের সাথে আলোচনা করুন।
-

জরিপের প্রশ্নের উত্তর দিন। এমনকি আপনি অধ্যয়নরত সমস্ত নথিতে আপনার অভিভূত হওয়ার ছাপ থাকলেও জেনে রাখুন যে আপনি যা ভাবেন তার চেয়ে বেশি ধারণাগুলি মুখস্থ করে রেখেছেন। অধ্যায়গুলির শেষে প্রশ্নের উত্তর দিন।- বেশিরভাগ পাঠ্যপুস্তক সঠিক উত্তরগুলি কীভাবে সন্ধান করতে হয় সে সম্পর্কে অন্যান্য তথ্য সরবরাহ করে। এটি আপনাকে আপনার যুক্তিতে কী কী মিস করেছে তা দেখার অনুমতি দেবে।
-

চিত্র, ছবি এবং টেবিল পরীক্ষা করুন। আপনি প্রায়শই পাঠ্যপুস্তকে ভিজ্যুয়াল দেখতে পাবেন যা মূল উপাদানগুলি মনে রাখতে আপনাকে আরও ভালভাবে বুঝতে সহায়তা করবে।- তাদের সাথে থাকা ছবি এবং ক্যাপশনগুলিকে ঘনিষ্ঠভাবে দেখুন। এটি আপনাকে কয়েকটি ধারণাটি বুঝতে সহায়তা করতে পারে।
-

কোর্স রেজিস্ট্রেশন করার অনুমতি জিজ্ঞাসা করুন। কারও নোটবুকে নোট নেওয়া কঠিন এবং একই সাথে বোর্ডে কী লেখা আছে তা দেখুন, বিশেষত রসায়নের মতো জটিল কোর্স। -

পুরানো প্রমাণ এবং পুরানো ম্যানুয়ালগুলি রাখার চেষ্টা করুন। বেশিরভাগ স্কুল পরীক্ষার্থীদের পরীক্ষার প্রস্তুতির জন্য পুরানো পরীক্ষার বৈধতা থাকতে দেয়।- উত্তরগুলি মুখস্ত করে এড়িয়ে চলুন। রসায়নে, আপনি যদি একই পদটির বিভিন্ন পদে উত্তর দিতে সক্ষম হতে চান তবে আপনাকে অবশ্যই ধারণাগুলি বুঝতে হবে।
-

অনলাইন সহায়তা সংস্থানগুলি দেখুন। আপনার প্রতিষ্ঠানের রসায়ন বিভাগ দ্বারা সরবরাহিত কোনও লিঙ্ক বা অনলাইন সংস্থান পরীক্ষা করে দেখুন।
পার্ট 2 পারমাণবিক কাঠামো বোঝা
-

সর্বাধিক প্রাথমিক কাঠামো দিয়ে শুরু করুন। রসায়ন পরীক্ষায় উত্তীর্ণ হওয়ার জন্য আপনাকে অবশ্যই এমন মৌলিক উপাদানগুলি বুঝতে হবে যা পদার্থ বা ভর রয়েছে এমন সমস্ত কিছু তৈরি করে।- রসায়নের সর্বাধিক মৌলিক উপাদানের কাঠামো বোঝা, অর্থাৎ লাতো এই শৃঙ্খলাটি বোঝার প্রথম পদক্ষেপ। সমস্ত বিষয় যা ক্লাসে অন্তর্ভুক্ত হবে তা এই প্রাথমিক তথ্যের একটি এক্সটেনশন হবে। পারমাণবিক রসায়ন বুঝতে প্রয়োজনীয় সময় নিন Take
-
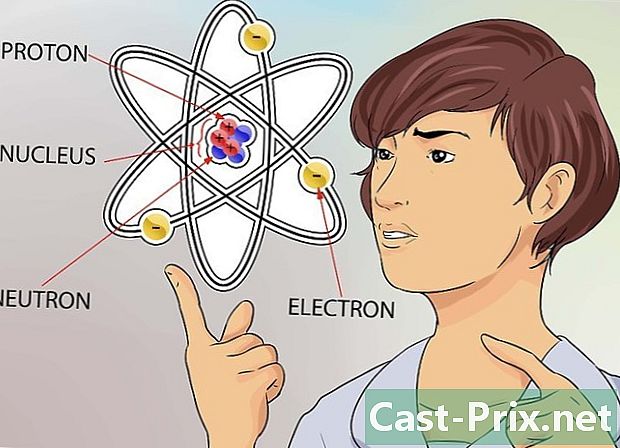
ডেটোম ধারণাটি বুঝুন। লাটোমকে আমরা সবসময় দেখতে পাই না এমন জিনিসগুলি, যেমন গ্যাসগুলি সহ সমস্ত বিষয়েই ক্ষুদ্রতম উপাদান হিসাবে বিবেচনা করা হয়। যাইহোক, এমনকি একটি ছোট পরমাণু এমনকি আরও ছোট কণা দ্বারা গঠিত যা এটির কাঠামো তৈরি করে।- পরমাণু নিউট্রন, প্রোটন এবং ইলেকট্রন দিয়ে গঠিত is ল্যাটোমের কেন্দ্রটিকে নিউক্লিয়াস বলা হয় এবং এটি নিউট্রন এবং প্রোটন দ্বারা গঠিত। গ্রহ যেমন সূর্যের চারদিকে ঘোরে তেমনি ইলেকট্রনগুলি সেই কণা যা ল্যাটোর চারপাশে মহাকর্ষণ করে।
- একটি পরমাণুর আকার অবিশ্বাস্যভাবে ছোট, তবে আপনাকে একটি তুলনা দিতে, আপনার জানা সবচেয়ে বড় স্টেডিয়ামটি ভাবার চেষ্টা করুন।আপনি যদি এই পর্যায়টিকে একটি পরমাণু হিসাবে বিবেচনা করেন তবে নিউক্লিয়াসটি ক্ষেত্রের কেন্দ্রে স্থাপন করা মটর সমান বড় হবে।
-
কোনও উপাদানের পারমাণবিক কাঠামো বুঝুন। শব্দটি উপাদান প্রাকৃতিকভাবে উদ্ভূত পদার্থ হিসাবে সংজ্ঞায়িত করা হয় যা অন্যান্য মৌলিক উপাদানগুলিতে ভেঙে ফেলা যায় না এবং এটি তার সরল আকারে। উপাদানগুলি ডেটোমগুলি নিয়ে গঠিত।- কোনও উপাদানে উপস্থিত পরমাণুগুলি সব একই হয়। এর অর্থ হ'ল প্রতিটি উপাদান তার পারমাণবিক কাঠামোর মধ্যে একটি নিউট্রন এবং প্রোটনগুলির একটি জ্ঞাত এবং অনন্য সংখ্যক রয়েছে।
-
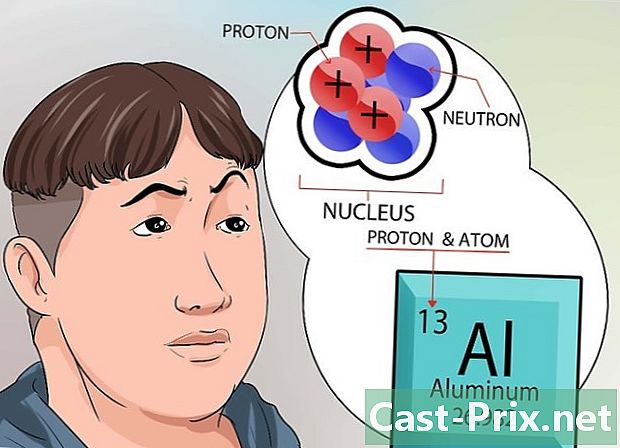
কার্নেল সম্পর্কে আরও জানুন। নিউক্লিয়াসে থাকা নিউট্রনগুলির একটি নিরপেক্ষ বৈদ্যুতিক চার্জ থাকে। অন্যদিকে প্রোটনগুলির একটি ইতিবাচক চার্জ রয়েছে। কোনও উপাদানের পারমাণবিক সংখ্যা তার নিউক্লিয়াসে উপস্থিত প্রোটনের সংখ্যার সাথে হুবহু মিলে যায়।- কোনও উপাদানটির প্রোটনের সংখ্যা জানতে আপনার গাণিতিক গণনা করার দরকার নেই। এই মান পর্যায় সারণীর প্রতিটি উপাদান প্রতিটি বক্সের শীর্ষে নির্দেশিত হয়।
-
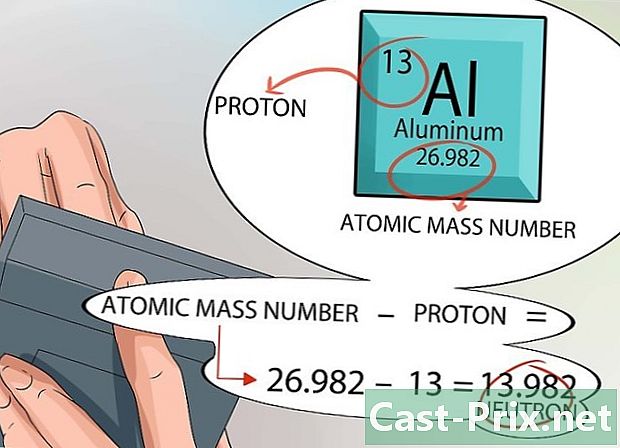
নিউক্লিয়াসে নিউট্রনের সংখ্যা গণনা করুন। আপনি এই উদ্দেশ্যে পর্যায় সারণীতে প্রদত্ত তথ্য ব্যবহার করতে পারেন। প্রতিটি উপাদানের পারমাণবিক সংখ্যা নিউক্লিয়াসে প্রোটনের সংখ্যার সমান।- পারমাণবিক ভর পর্যায় সারণীর প্রতিটি বাক্সে নির্দেশিত হয় এবং কেবলমাত্র উপাদানটির নাম অনুসারে নীচে থাকে।
- মনে রাখবেন যে কেবলমাত্র প্রোটন এবং নিউট্রন নিউক্লিয়াসে থাকে। পর্যায় সারণীর সাহায্যে আপনি কোনও রাসায়নিক উপাদানের প্রোটন সংখ্যা এবং পারমাণবিক ভর জানতে পারবেন।
- এই মুহুর্তে, গণনাটি বেশ সহজ। সেই উপাদানটির ল্যাটোমে নিউক্লিয়াসে নিউট্রনের সংখ্যা খুঁজতে কেবল পারমাণবিক ভর থেকে প্রোটনের সংখ্যা বিয়োগ করুন।
-
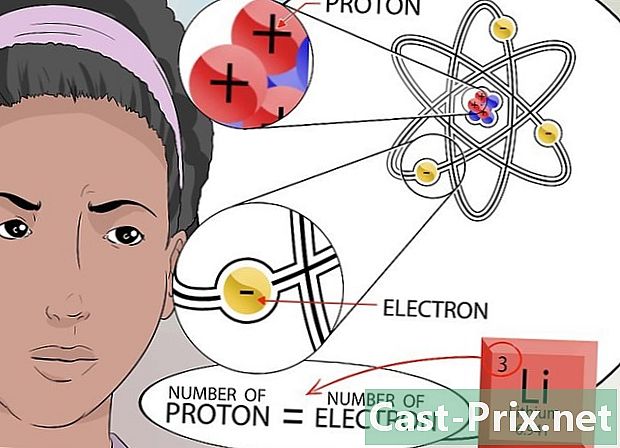
ইলেক্ট্রনের সংখ্যা নির্ধারণ করুন। মনে রাখবেন যে বিপরীত উপাদানগুলি সঠিক। গ্রহ যেমন সূর্যের চারদিকে ঘোরে তেমনি ইলেক্ট্রনগুলি নিউক্লিয়াসের চারদিকে ঘোরে negativeণাত্মক চার্জযুক্ত কণা। নিউক্লিয়াসের প্রতি আকৃষ্ট ইলেক্ট্রনগুলির সংখ্যা (নেতিবাচক চার্জ সহ) নিউক্লিয়াসে উপস্থিত প্রোটনের সংখ্যার (ধনাত্মক চার্জ সহ) নির্ভর করে।- যেহেতু ল্যাটোমের শূন্য মোট চার্জ রয়েছে তাই সমস্ত ধনাত্মক এবং নেতিবাচক চার্জগুলি ভারসাম্যপূর্ণ হওয়া উচিত। এই কারণে, ইলেক্ট্রনের সংখ্যা প্রোটনের সংখ্যার সমান।
-
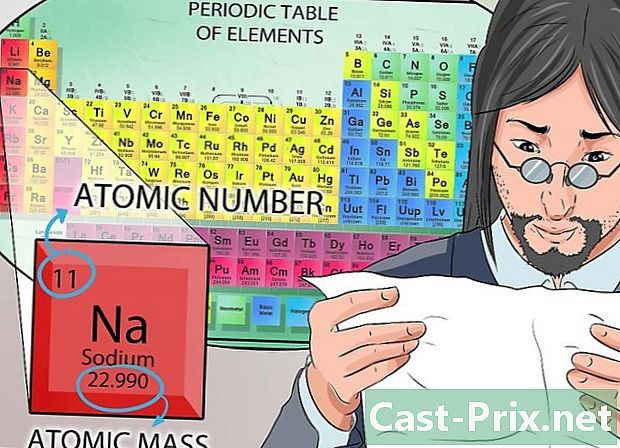
পর্যায় সারণী পর্যবেক্ষণ করুন। রাসায়নিক উপাদানগুলির বৈশিষ্ট্যগুলি বুঝতে যদি আপনার সমস্যা হয় তবে পর্যায় সারণীতে উপলব্ধ সমস্ত তথ্য পর্যালোচনা করার জন্য সময় নিন take সবচেয়ে গুরুত্বপূর্ণ, চার্টটি সাবধানে অধ্যয়ন করুন study- আপনার কেমিস্ট্রি ক্লাসের প্রথম অংশের সাফল্যের জন্য এই চার্টটি বোঝা অপরিহার্য।
- পর্যায় সারণীতে কেবলমাত্র উপাদান থাকে। প্রতিটি দুটি এক বা দুটি প্রতীক দ্বারা প্রতিনিধিত্ব করা হয়। প্রতীকটি উপাদানটিকে স্বতন্ত্রভাবে চিহ্নিত করে। উদাহরণস্বরূপ, প্রতীক নার সর্বদা মানে সোডিয়াম ল্যাটোম। রাসায়নিক উপাদানটির পুরো নামটি সাধারণত চিহ্নের নিচে লেখা হয়।
- প্রতীকের পারমাণবিক সংখ্যাটি উপরে ছাপা সংখ্যা দ্বারা প্রতিনিধিত্ব করা হয়। পারমাণবিক সংখ্যা নিউক্লিয়াসে প্রোটনের সংখ্যার সমান।
- প্রতীকের নীচে সংখ্যাটি পারমাণবিক ভরের সাথে মিলে যায়। এটি ভুলে যাবেন না: একটি পরমাণুর ভর সংখ্যা নিউক্লিয়াসে থাকা প্রোটন এবং নিউট্রনের যোগফলের সমান।
-
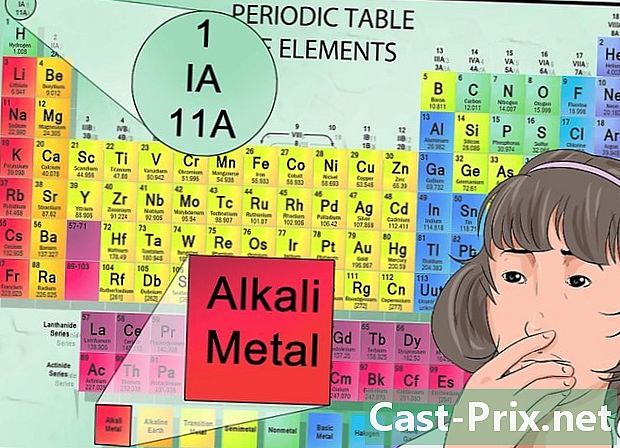
পর্যায় সারণির ব্যাখ্যা করুন। পর্যায় সারণীতে প্রচুর তথ্য রয়েছে, প্রতিটি কলামের রঙ এবং বাম থেকে ডানে এবং উপরে থেকে নীচে পর্যন্ত উপাদানগুলির অবস্থান সহ।
পার্ট 3 রাসায়নিক প্রতিক্রিয়ার পূর্বাভাস
-

রাসায়নিক সমীকরণের ভারসাম্য রক্ষা করুন। রসায়নে, আপনাকে ভবিষ্যদ্বাণী করতে হবে উপাদানগুলি একে অপরের সাথে কীভাবে প্রতিক্রিয়া দেখায়। অন্য কথায়, আপনাকে অবশ্যই রাসায়নিক বিক্রিয়াকে ভারসাম্য রাখতে সক্ষম হতে হবে।- রাসায়নিক সমীকরণে, রিএজেন্টগুলি বামদিকে অবস্থিত এবং তারপরে একটি তীর প্রতিক্রিয়ার পণ্যগুলি নির্দেশ করে ডানদিকে নির্দেশ করে। এবং সমীকরণের প্রতিটি পক্ষের উপাদানগুলি ভারসাম্যপূর্ণ হতে হবে।
- উদাহরণস্বরূপ, রিএজেন্ট 1 + রিএজেন্ট 2 → প্রোডাক্ট 1 + প্রোডাক্ট 2।
- এখানে টিনের প্রতীকগুলির সাথে একটি উদাহরণ রয়েছে, যার প্রতীক স্ন Sn টিন ডাই অক্সাইড (স্নো 2) কে গ্যাসীয় আকারে (এইচ 2) হাইড্রোজেনের সাথে একত্রিত করুন। সমীকরণটি SnO2 + H2 → Sn + H2O।
- তবে, এই সমীকরণটি ভারসাম্যপূর্ণ নয়, যেহেতু রিজেন্টগুলির পরিমাণ পণ্যগুলির সাথে সমান নয়। প্রতিক্রিয়ার ডান পাশের চেয়ে বাম পাশে আরও একটি অক্সিজেন পরমাণু রয়েছে।
- সাধারণ গাণিতিক গণনা ব্যবহার করে, আপনি বামদিকে দুটি হাইড্রোজেন ইউনিট এবং ডানদিকে দুটি পানির অণু রেখে সমীকরণটি ভারসাম্যপূর্ণ করতে পারেন। একবারে ভারসাম্যযুক্ত প্রতিক্রিয়াটি হ'ল: SnO2 + 2 H2 → Sn + 2 H2O।
-
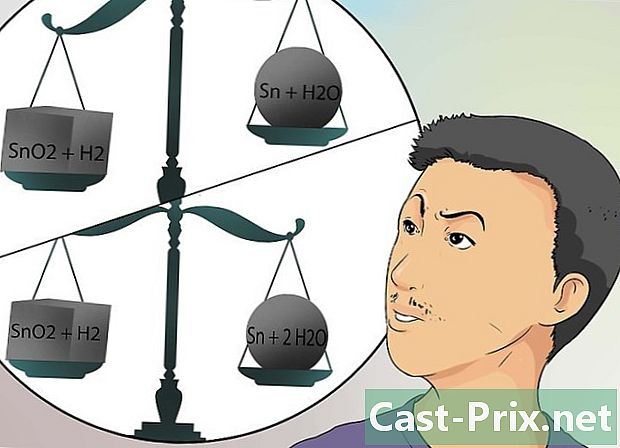
সমীকরণগুলি আলাদাভাবে চিন্তা করুন। রাসায়নিক বিক্রিয়াগুলিগুলিকে ভারসাম্য বজায় রাখতে আপনার যদি সমস্যা হয়, তবে কোনও রেসিপিটির কোন অংশটি কল্পনা করুন তবে আপনার রেসিপিটির চূড়ান্ত পণ্য কম-বেশি পেতে সামঞ্জস্য করতে হবে।- সমীকরণটি আপনাকে সমীকরণের বাম দিকে উপাদান সরবরাহ করে তবে আপনাকে ডোজ সম্পর্কে তথ্য দেয় না। যাইহোক, সমীকরণটি আপনাকে পণ্য হিসাবে কী পেতে চলেছে তা জানতে দেয়, সর্বদা পরিমাণগুলি বাদ দেয়। এবং আপনি তাদের খুঁজে পেতে হবে।
- সর্বদা উপরের উদাহরণটি ব্যবহার করে (স্নো 2 + এইচ 2 → সান + এইচ 2 ও), কেন এই প্রতিক্রিয়াটি (বা রেসিপিটির সূত্রটি) কাজ করে না তা বিবেচনা করুন। সমীকরণের উভয় দিকের টিনের (এসএন) পরিমাণ সমান, হাইড্রোজেন (এইচ 2) এর পরিমাণও। তবে, বাম দিকে আমাদের অক্সিজেনের 2 টি এবং ডানদিকে কেবল 1 রয়েছে।
- H2O (2 H2O) এর দুটি অণু রয়েছে তা বোঝাতে সমীকরণের ডান দিকটি পরিবর্তন করুন। সামনে 2 নম্বর H2O এর অর্থ এই অণুর সমস্ত পরমাণু এখন দ্বিগুণ হয়ে গেছে। এখন, অক্সিজেনের পরিমাণ সুষম, তবে হাইড্রোজেনের নয়, কারণ ডানদিকে বামের চেয়ে বেশি হাইড্রোজেন রয়েছে। এই কারণে, আমাদের অবশ্যই সমীকরণের বাম দিকে ফিরে যেতে হবে। এইচ 2 উপাদানের পরিমাণ সংশোধন করুন এবং এইচ 2 এর সামনে একটি গুণফল 2 রেখে তাদের দ্বিগুণ করুন।
- এবং এখানে আপনি সমীকরণের উভয় পক্ষের উপাদানের সমস্ত ডোজকে ভারসাম্যপূর্ণ করছেন। আপনার রেসিপির উপাদানগুলি প্রাপ্ত পণ্যগুলির মতো একই (তাই ভারসাম্যপূর্ণ)।
-
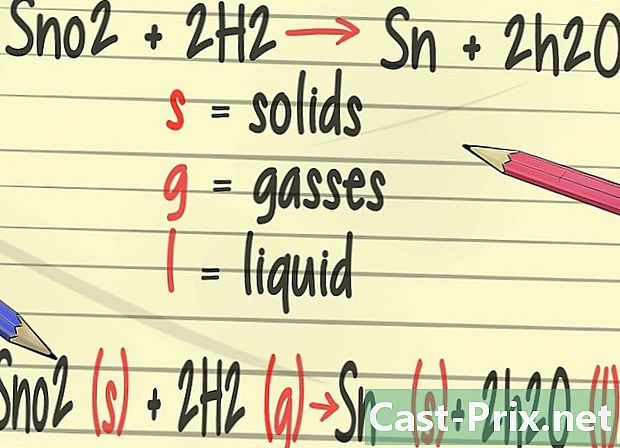
সুষম সমীকরণে আরও বিশদ যুক্ত করুন। রসায়নে আপনি উপাদানগুলির শারীরিক অবস্থার প্রতিনিধিত্বকারী চিহ্নগুলি যুক্ত করতে শিখবেন। চিঠি গুলি কঠিন, চিঠি প্রতীক ছ গ্যাস এবং অক্ষর জন্য ব্যবহৃত হয় ঠ তরল প্রতিনিধিত্ব করে। -
একটি প্রতিক্রিয়া চলাকালীন পরিবর্তনগুলি সনাক্ত করুন। রাসায়নিক বিক্রিয়াগুলি প্রথমে মৌলিক উপাদানগুলি বা ইতিমধ্যে সংযুক্ত উপাদানগুলিকে রিএজেন্টসকে প্রভাবিত করে। দুই বা ততোধিক রিএজেন্টের সংমিশ্রণ এক বা একাধিক পণ্য বাড়ে।- রসায়ন পরীক্ষায় উত্তীর্ণ হওয়ার জন্য আপনাকে অবশ্যই সমীকরণগুলি সমাধান করতে সক্ষম হতে হবে যা রিএজেন্টস, পণ্যগুলিকে জড়িত এবং তাদের আচরণকে প্রভাবিত করে এমন অন্যান্য কারণগুলিকেও বিবেচনায় নিতে পারে।
-
বিভিন্ন ধরণের প্রতিক্রিয়া অধ্যয়ন করুন। রাসায়নিক প্রতিক্রিয়া কারণগুলির একমাত্র সংমিশ্রণের বাইরে চলে যায় এমন অনেকগুলি কারণের কারণে ঘটে।- রসায়নের বিষয়ে অধ্যয়ন করা এবং আপনার জানা উচিত এমন সাধারণ প্রতিক্রিয়াগুলি হ'ল: সংশ্লেষণের প্রতিক্রিয়া, প্রতিস্থাপন, অ্যাসোডাবাসিক প্রতিক্রিয়া, জারণ হ্রাস, দহন, জলবিদ্যুণ, পচন, মেটাথিসিস এবং ডিসোমাইজারেশন।
- রসায়ন ক্লাস চলাকালীন, আপনার শিক্ষক প্রোগ্রামের উপর নির্ভর করে অন্যান্য ধরণের প্রতিক্রিয়াও উপস্থাপন করতে পারেন। স্পষ্টতই, উচ্চ বিদ্যালয়ের রসায়ন প্রোগ্রামটি বিশ্ববিদ্যালয়ে যে প্রোগ্রামটি শেখানো হয় তার মতো বিশদ হবে না।
-

আপনার কাছে উপলব্ধ সমস্ত সংস্থান ব্যবহার করুন। ক্লাসে সম্বোধন করা প্রতিটি ধরণের প্রতিক্রিয়ায় আপনাকে অবশ্যই পার্থক্যগুলি সনাক্ত করতে সক্ষম হতে হবে। আপনার এই ধারণাগুলি বুঝতে হবে এমন সমস্ত অধ্যয়নের সংস্থানগুলি ব্যবহার করুন এবং শ্রেণিতে প্রশ্ন জিজ্ঞাসা করতে দ্বিধা করবেন না।- প্রতিক্রিয়াগুলির মধ্যে পার্থক্যগুলি কখনও কখনও শিক্ষার্থীদের জন্য বিভ্রান্তি তৈরি করতে পারে এবং রাসায়নিক বিক্রিয়াকালীন ঘটে যাওয়া বিভিন্ন প্রক্রিয়া বোঝা পুরো কোর্সের সবচেয়ে জটিল অংশ হতে পারে।
-

যৌক্তিকভাবে রাসায়নিক প্রতিক্রিয়াগুলি বোঝেন। প্রক্রিয়াটি ইতিমধ্যে যত জটিল হয়েছে তার চেয়ে বেশি জটিল করবেন না, সাধারণ শর্তাবলী দ্বারা বিভ্রান্ত রেখে। আপনি যে সমস্ত প্রতিক্রিয়া অধ্যয়ন করবেন তার মধ্যে আপনাকে কেবল কিছু অন্য কিছুতে পরিণত করতে হবে।- উদাহরণস্বরূপ, আপনি ইতিমধ্যে জানেন যে অক্সিজেনের একটি অণুর সাথে হাইড্রোজেনের দুটি অণু মিশ্রিত করে আপনি জল পান। অতএব, আপনি যদি সসপ্যানে জল andালেন এবং এটি আগুনে রাখেন, তবে কিছু পরিবর্তন হবে। আপনি আসলে একটি রাসায়নিক বিক্রিয়া তৈরি করেছেন। আপনি যদি ফ্রিজে জল রাখেন তবে কিছু ঘটবে। সংক্ষেপে, আপনি একটি ফ্যাক্টর প্রবর্তন করেছেন যা প্রাথমিক রিএজেন্টের অবস্থার পরিবর্তন করে এবং আমাদের ক্ষেত্রে এটি জল।
- প্রতিটি প্রতিক্রিয়া বিভাগকে একে একে আয়ত্ত না করা পর্যন্ত পুনরায় লিখুন, তারপরে পরবর্তীটিতে যান। শক্তির উত্সের দিকে মনোনিবেশ করুন যা প্রতিক্রিয়া সৃষ্টি করে এবং যে বড় পরিবর্তনগুলি ঘটে।
- আপনি যদি এই ধারণাগুলি বুঝতে না পারেন, তবে আপনার শিক্ষক, আপনার অধ্যয়ন গোষ্ঠী, বা কেমিস্ট্রিতে বেশ ভাল কেউ এমন ব্যক্তির সাথে আপনি যা বোঝেন না এবং সেগুলি নিয়ে আলোচনা করেন না তার একটি তালিকা তৈরি করুন।
অংশ 4 রসায়নে গণিত প্রয়োগ করা
-

বেসিক গণনার ক্রম শিখুন। রসায়নে, কখনও কখনও খুব বিস্তারিত গণনা করা প্রয়োজন, তবে অন্যান্য সময়ে, মৌলিক ক্রিয়াকলাপগুলি যথেষ্ট। যাইহোক, সমীকরণগুলি সম্পূর্ণ করতে এবং সমাধান করার জন্য ক্রিয়াকলাপগুলির সঠিক ক্রমটি জানা প্রয়োজনীয়।- একটি সহজ সংক্ষিপ্ত বিবরণ মুখস্ত করুন। শিক্ষার্থীরা নির্দিষ্ট ধারণাটি মুখস্ত করতে বিভিন্ন বাক্য ব্যবহার করে এবং গাণিতিক ক্রিয়াকলাপের ক্রমও এর ব্যতিক্রম নয়। পেমডাস নামটির সাথে (যা হতে পারে আমার শেষ এএস) শব্দটি থেকে উদ্ভূত, আপনি সহজেই মনে করতে পারেন কোন গাণিতিক ক্রিয়াকলাপ সম্পাদন করতে হবে। প্রতিটি শব্দের প্রথম অক্ষর প্রতিটি ক্রমের ক্রম নির্দেশ করে। প্রথমে প্যারেন্টিজেস, তারপরে প্রদর্শক, গুণ, বিভাগ, সংযোজন এবং অবশেষে বিয়োগফলগুলিতে সবকিছু করুন।
- PEMDAS নাম দ্বারা নির্দেশিত ক্রিয়াকলাপ অনুসরণ করে 3 + 2 x 2 x 6 = ___ এই অভিব্যক্তিটির জন্য গণনাগুলি সম্পাদন করুন। সমাধান 15।
-

কীভাবে খুব বড় মূল্যবোধ তৈরি করতে হয় তা শিখুন। যদিও রাউন্ডিং সংখ্যাগুলি রসায়নে খুব সাধারণ বিষয় না, তবে কখনও কখনও কিছু জটিল গাণিতিক সমীকরণের সমাধান লিখতে খুব দীর্ঘ হয়। আপনার উত্তরগুলি গোল করা উচিত কিনা তা জানতে আপনি যে অনুশীলনের উপর কাজ করছেন সেগুলির নির্দেশগুলি মনোযোগ সহকারে পড়ুন।- কখন উপরে বা নিচে নামতে হবে তা শিখুন। একটি সাংখ্যিক ক্রমের মধ্যে, যদি পরবর্তী অঙ্কটি 4 এর চেয়ে কম বা সমান হয়, তবে নীচে। এবং যদি এটি 5 এর চেয়ে বড় বা সমান হয় তবে পরের সংখ্যাটিতে গোল করুন। আসুন এই সংখ্যাটির 6, 66 666 666 666 666 উদাহরণটি ধরুন। ধরুন আপনাকে দ্বিতীয় দশমিক স্থানে বাঁকতে হবে। উত্তরটি 6.67 হবে।
-
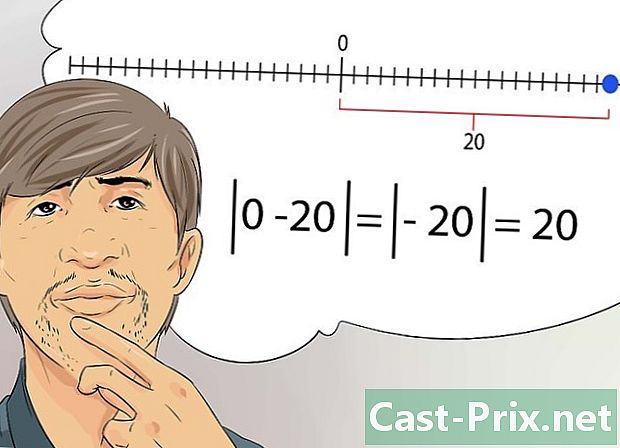
পরম মানের ধারণা বুঝতে। রসায়নে কিছু সংখ্যাকে নিখুঁত মান হিসাবে উল্লেখ করা হয়, না প্রকৃত গাণিতিক মান হিসাবে। একটি বাস্তব x এর পরম মানটি এই সংখ্যা x এবং শূন্যের মধ্যবর্তী দূরত্ব।- অন্য কথায়, আপনাকে আর সংখ্যার চিহ্ন (ধনাত্মক বা negativeণাত্মক) বিবেচনা করার দরকার নেই, বরং এটির শূন্যের দূরত্ব। উদাহরণস্বরূপ, -20 এর পরম মান 20 হয়।
-
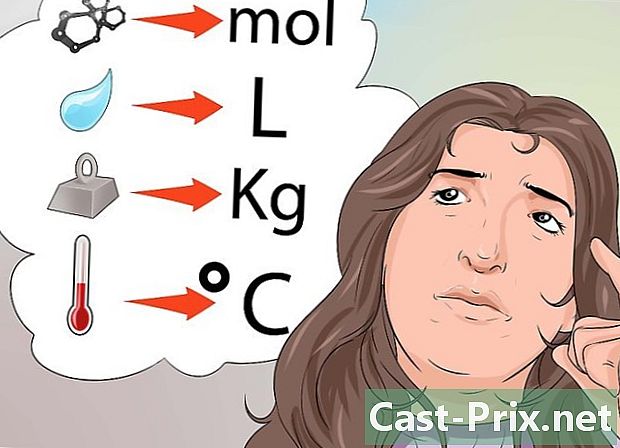
পরিমাপের স্বীকৃত ইউনিটগুলির সাথে নিজেকে পরিচিত করুন। এখানে কিছু উদাহরণ।- উপাদানের পরিমাণ মোলগুলিতে প্রকাশিত হয় (মোল)।
- তাপমাত্রা ডিগ্রি সেলসিয়াস (ডিগ্রি সেন্টিগ্রেড), ফারেনহাইট (° ফ) বা কেলভিন (° কে) দিয়ে প্রকাশ করা হয়।
- ভর গ্রাম (ছ), কিলোগ্রাম (কেজি) বা মিলিগ্রাম (মিলিগ্রাম) দ্বারা প্রকাশিত হয়।
- ভলিউম এবং তরলগুলি লিটার (এল) বা মিলিলিটারগুলিতে প্রকাশিত হয় (মিলি)।
-

কীভাবে মানগুলি একটি পরিমাপের স্কেল থেকে অন্যটিতে রূপান্তর করতে হয় তা শিখুন। আপনার রসায়ন পরীক্ষায় উত্তীর্ণ হওয়ার জন্য, আপনাকে একটি স্বীকৃত স্কেল থেকে অন্যটিতে কিছু রূপান্তর করতে সক্ষম হতে হবে। উদাহরণস্বরূপ, আপনাকে এক তাপমাত্রা পরিমাপ থেকে অন্যটিতে যেতে হতে পারে, কেজি কেজি পাউন্ড বা লিটারে তরল আউনে রূপান্তর করতে হবে।- কখনও কখনও আপনাকে মূল ইউনিট থেকে পৃথক পরিমাপের একটি ইউনিটে সমস্যার সমাধান প্রকাশ করতে বলা হবে। উদাহরণস্বরূপ, ধরুন আপনাকে কোনও তাপমাত্রা সমীকরণ সমাধান করতে হবে যার মানগুলি সেলসিয়াসে রয়েছে তবে আপনার চূড়ান্ত উত্তরটি অবশ্যই কেলভিনে থাকতে হবে।
- ক্যালভিন হ'ল তাপমাত্রা পরিমাপের আন্তর্জাতিক মানের যা ঘন ঘন রাসায়নিক বিক্রিয়ায় ব্যবহৃত হয়। ডিগ্রি সেলসিয়াস থেকে ডিগ্রি কেলভিন বা ডিগ্রি ফারেনহাইটে যাওয়ার অনুশীলন করুন।
-
কিছু সময় ব্যায়াম করতে ব্যয় করুন। আপনি ক্লাসে বেশ কয়েকটি ধারণা অধ্যয়ন করার সময়, কীভাবে একক থেকে অন্য ব্যবস্থায় পরিমাপের একক রূপান্তর করতে হয় তা শিখতে সময় নিন। -

ঘনত্বের গণনা কীভাবে করবেন তা শিখুন। শতাংশ, অনুপাত এবং অনুপাত সম্পর্কে আপনার প্রাথমিক জ্ঞানকে আরও গভীর করুন। -

পুষ্টির লেবেলগুলির সাথে অনুশীলন করুন। আপনার রসায়ন পরীক্ষায় উত্তীর্ণ হওয়ার জন্য, আপনাকে সহজেই অনুপাত, শতাংশ, অনুপাত এবং তাদের বিপরীত ক্রিয়াকলাপ গণনা করতে সক্ষম হওয়া উচিত। যদি আপনি এই ধারণাগুলি ভালভাবে বুঝতে না পারেন, তবে আপনাকে অন্যান্য পরিমাপের ইউনিটগুলির সাথে প্রশিক্ষণের দরকার যা পুষ্টির লেবেলের মতো common- যে কোনও খাদ্য পণ্যের পুষ্টি লেবেল পরীক্ষা করুন। আপনি প্রতি পরিবেশিত ক্যালোরি, প্রস্তাবিত দৈনিক গ্রহণের শতাংশ, মোট চর্বিযুক্ত সামগ্রীর পরিমাণ, চর্বিযুক্ত ক্যালোরির পরিমাণ, মোট শর্করা জাতীয় উপাদান এবং বিভিন্ন ধরণের কার্বোহাইড্রেটের বিচ্ছেদ খুঁজে পাবেন। ডিনোমিনিটার হিসাবে বিভিন্ন বিভাগের মানগুলি থেকে কীভাবে বিভিন্ন শতাংশের গণনা করা যায় তা শিখুন।
- উদাহরণস্বরূপ, কোনও পণ্যের মোট ফ্যাটের পরিমাণের তুলনায় মনস্যাচুরেটেড ফ্যাটের পরিমাণ গণনা করুন। মানকে শতাংশে রূপান্তর করুন। প্যাকেজটিতে প্রতি ক্যালোরির সংখ্যা এবং অংশের পরিমাণ ব্যবহার করে পণ্যটিতে ক্যালোরির সংখ্যা গণনা করুন। প্যাকেজজাত পণ্যের অর্ধেক পরিমাণে সোডিয়াম উপস্থিত পরিমাণ গণনা করুন।
- এই ধরণের রূপান্তরগুলির সাথে প্রশিক্ষণ দ্বারা, আপনি যে কোনও পরিমাপের ইউনিট ব্যবহার করেন না কেন আপনি সহজেই পরিমাপের ইউনিটগুলিকে রাসায়নিক পরিমাণে যেমন লিটার প্রতি তিল, মোল প্রতি গ্রাম এবং আরও অনেক কিছুতে রূপান্তর করতে পারেন।
-

অ্যাভোগাড্রোর নম্বর কীভাবে ব্যবহার করবেন তা শিখুন। এই ধ্রুবক একটি তিলতে থাকা অণু, ডেটোম বা কণার সংখ্যা উপস্থাপন করে। অ্যাভোগাড্রোর সংখ্যা 6,022 x 1023।- উদাহরণস্বরূপ, ফে এর 0.450 মলে কয়টি ডেটোম রয়েছে? উত্তর 0.450 x 6 022 x 1023।
-
গাজরের কথা ভাবুন। রসায়নের সমস্যায় যদি অ্যাভোগাড্রোর সংখ্যা প্রয়োগ করতে সমস্যা হয় তবে অণু, অণু বা কণার চেয়ে গাজরের কথা চিন্তা করুন। এক ডজনে কতটি গাজর রয়েছে? এক ডজনে 12 টি উপাদান রয়েছে, তাই এক ডজনে 12 টি গাজর রয়েছে।- এখন, এই প্রশ্নের উত্তর দেওয়ার চেষ্টা করুন: একটি তিলতে কয়টি গাজর রয়েছে? 12 দ্বারা গুণনের পরিবর্তে, অ্যাভোগাড্রোর সংখ্যাটি ব্যবহার করুন। একটি তিলতে 6,022 x 1,023 কোর রয়েছে।
- অ্যাভোগাড্রোর সংখ্যা রাসায়নিক পরিমাণকে (মোলের সংখ্যা) বিভিন্ন সংখ্যায় (একটি পরমাণু, একটি অণু, একটি কণা বা একটি গাজর) রূপান্তর করতে ব্যবহৃত হয়।
- যদি আপনি কোনও উপাদানের মোলের সংখ্যা জানেন তবে আপনি এভোগাড্রোর ধ্রুবতকে প্রশ্নের উত্তর দিয়ে সংখ্যাকে গুণ করে এই পরিমাণে পদার্থের অণু, ডেটোম বা কণার সংখ্যা জানতে পারবেন।
- রসায়নে আপনার পরীক্ষায় উত্তীর্ণ হওয়ার জন্য কীভাবে তিলকে কণাগুলি রূপান্তর করতে হয় তা বোঝা গুরুত্বপূর্ণ। অনুপাত এবং শতাংশ গণনা করার জন্য, আপনাকে মোলার রূপান্তর করতে হবে। অন্য কথায়, আপনাকে অবশ্যই অন্য এককের তুলনায় তিলতে প্রকাশিত উপাদানের পরিমাণ জানতে হবে।
-
আনুষঙ্গিকতার ধারণাটি বোঝার চেষ্টা করুন। তরল মাধ্যমের মধ্যে দ্রবীভূত কোনও পদার্থের মলের সংখ্যা বিবেচনা করুন। এটি বোঝার জন্য এটি একটি অত্যন্ত গুরুত্বপূর্ণ উদাহরণ কারণ এটি তাত্পর্য, এটি প্রতি লিটার মলে প্রকাশিত কোনও রাসায়নিক প্রজাতির অনুপাত।- রসায়নে, তরল মাধ্যমের মধ্যে থাকা কোনও পদার্থের পরিমাণ বা তরল দ্রবণের মধ্যে থাকা দ্রবণের পরিমাণ প্রকাশ করার জন্য দুরত্ব ব্যবহার করা হয়। আপনি দ্রবণের মোলের সংখ্যাটি লিটারে দ্রবণের পরিমাণ দ্বারা ভাগ করে আপনি নির্জনতা গণনা করতে পারেন। এর পরিমাপের এককটি প্রতি লিটার মোল (মোল / এল)।
- ঘনত্ব গণনা করুন। ঘনত্বও রসায়নের ক্ষেত্রে সাধারণত ব্যবহৃত একটি পরিমাপ। এটি রাসায়নিক পদার্থের প্রতি ইউনিট ভলিউমকে প্রকাশ করে। এখানে পরিমাপের সর্বাধিক সাধারণ ইউনিট হ'ল গ্রাম প্রতি লিটার (g / l) বা প্রতি ঘন সেন্টিমিটার (গ্রাম / সেমি 3) গ্রাম gram
-

সমীকরণগুলিকে তাদের অভিজ্ঞতামূলক সূত্রে হ্রাস করুন। অন্য কথায়, আপনার সমীকরণের চূড়ান্ত সমাধানগুলি ভুল হিসাবে বিবেচিত হবে যদি আপনি সেগুলিকে তাদের সহজতম ফর্মের তুলনায় হ্রাস না করেন।- এটি আণবিক সূত্রে প্রযোজ্য নয় কারণ এই ধরণের বিবরণটি অণু তৈরির রাসায়নিক উপাদানগুলির মধ্যে সঠিক অনুপাত নির্দেশ করে।
-

আণবিক সূত্রের ধারণাটি বুঝুন। আপনাকে কোনও আণবিক সূত্রকে এর সর্বাধিকতম আকারে বা অভিজ্ঞতাগতভাবে হ্রাস করার প্রয়োজন হবে না কারণ এটি অণুর গঠনটি হুবহু প্রকাশ করে।- কোনও দেহের আণবিক সূত্র লেখার জন্য রাসায়নিক উপাদানগুলির সংক্ষিপ্তসার পাশাপাশি অণুতে প্রতিটি উপাদানের সংখ্যা ডেটোমগুলি ব্যবহার করা।
- ধরুন জলের আণবিক সূত্র, এইচ 2 ও। পানির প্রতিটি অণু হাইড্রোজেনের দুটি পরমাণু এবং অক্সিজেনের একটি পরমাণু নিয়ে গঠিত। ল্যাসেটামিনোফেন, সি 8 এইচ 9 এনও 2 এর আণবিক সূত্রের সাথে এটি করার চেষ্টা করুন। আসলে, সমস্ত রাসায়নিক যৌগগুলি তাদের আণবিক সূত্রগুলির দ্বারা প্রতিনিধিত্ব করা হয়।
-

স্টোচিওমিট্রি সম্পর্কে আরও জানুন। আপনি সম্ভবত এই পদটি পূরণ করবেন। স্টোইচিওমিট্রি হ'ল গাণিতিক সূত্রগুলি ব্যবহার করে রাসায়নিক বিক্রয়ের পরিমাণগত অনুপাতের অধ্যয়ন। স্টোচিওমিট্রি (গণিতটি রসায়নের ক্ষেত্রে প্রয়োগ করা হয়), উপাদান এবং রাসায়নিক যৌগের মানগুলি সাধারণত মোলগুলিতে, মোলার শতাংশে, প্রতি লিটার মলে বা প্রতি কেজি মলে প্রতিনিধিত্ব করে।- গাণিতিক ক্রিয়াকলাপগুলির মধ্যে একটি হ'ল গ্রামকে মলে রূপান্তর করা। কোনও উপাদানটির পারমাণবিক ভর ইউনিট, সাধারণত গ্রামে প্রকাশিত হয়, এই পদার্থের একটি তিলের সাথে মিল রয়েছে। উদাহরণস্বরূপ, ক্যালসিয়াম ল্যাটোম ভর 40 পারমাণবিক ভর ইউনিট। সুতরাং, 40 গ্রাম ক্যালসিয়াম ক্যালসিয়ামের একটি তিল সমান।
-

অতিরিক্ত অনুশীলনের জন্য শিক্ষককে জিজ্ঞাসা করুন। গাণিতিক সমীকরণ এবং রূপান্তর যদি সমস্যা হয় তবে শিক্ষকের সাথে কথা বলুন। যতক্ষণ না আপনি সমস্ত ব্যবহৃত ধারণাটি স্পষ্টভাবে বুঝতে না পারছেন ততক্ষণ নিজেকে নিজেকে আরও বেশি অনুশীলন করতে বলুন।
পর্ব 5 রসায়নের ভাষা ব্যবহার করে
-
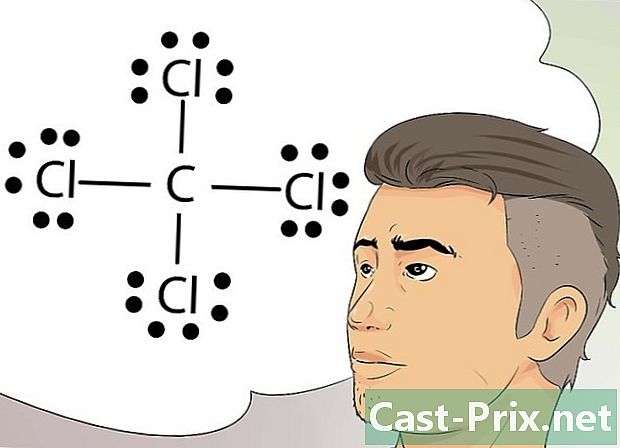
লুইসের কাঠামো সনাক্ত করুন। এই কাঠামোগুলি, যাকে লুইস সূত্রও বলা হয়, এটি কোনও পরমাণুর বাইরের স্তরে দলবদ্ধ ইলেকট্রন এবং একক ইলেকট্রনকে উপস্থাপন করতে বিন্দু ব্যবহারের গ্রাফিকাল উপস্থাপনা।- এই কাঠামোগুলি সাধারণ চিত্রগুলি আঁকার জন্য এবং সমবায় বাঁধাগুলির মতো বন্ডগুলি সনাক্ত করতে খুব কার্যকর যা বিভিন্ন উপাদান একটি পরমাণু বা একটি অণুতে ভাগ করে দেয়।
-

লকেট বিধি জানুন। লুইসের কাঠামো এই নিয়মের উপর ভিত্তি করে তৈরি করা হয়েছে, যা বলে যে পরমাণুগুলি স্থিতিশীল থাকে যখন তাদের বাইরের স্তরটিতে ঠিক 8 টি ইলেক্ট্রন থাকে। এই নিয়মের ব্যতিক্রম হিসাবে, হাইড্রোজেনকে তার বাইরের স্তরে 2 টি ইলেক্ট্রন দিয়ে স্থিতিশীল হিসাবে বিবেচনা করা হয়। -
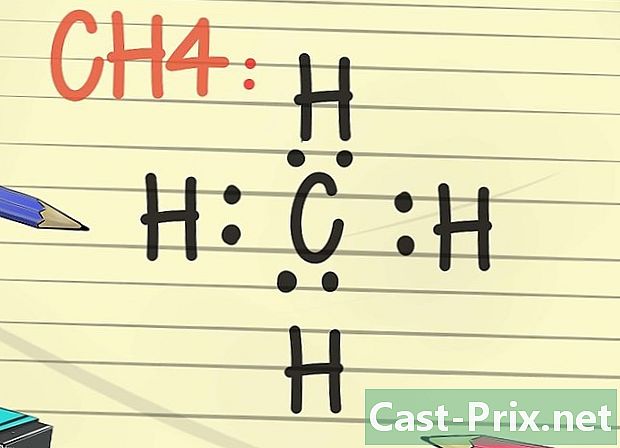
একটি লুইস কাঠামো আঁকুন। এই কাঠামোটি বিন্দুগুলির একটি ধারা দ্বারা বেষ্টিত একটি উপাদানটির প্রতীক দ্বারা প্রতিনিধিত্ব করা হয়। ভাবুন এটি কোনও সিনেমার ক্যাপচারিত স্থির চিত্র। নিউক্লিয়াসের চারপাশে মাধ্যাকর্ষণকারী ইলেক্ট্রনগুলির পরিবর্তে আমরা একটি নির্দিষ্ট মুহুর্তে তাদের অবস্থানের প্রতিনিধিত্ব করি।- লুইস কাঠামো ইলেক্ট্রনগুলির সবচেয়ে স্থিতিশীল বিন্যাস, অন্য রাসায়নিক উপাদানগুলির সাথে তাদের সংযোগের অবস্থানগুলি কল্পনা করতে দেয়। এটি বন্ড শক্তির উপরও তথ্য সরবরাহ করে (উদাহরণস্বরূপ, তারা সমবায় বা দ্বিগুণ)।
- বাইট রুলটিকে বিবেচনায় নিয়ে লুইস কার্বন স্ট্রাকচার (সি) আঁকার চেষ্টা করুন। ল্যাটোমের প্রতিটি পাশে 2 টি পয়েন্ট রাখুন (উপরে, নীচে, বাম এবং ডানদিকে)। এবার প্রতিটি জোড়া বিন্দুর অন্যদিকে একটি এইচ, হাইড্রোজেন ল্যাটোম প্রতীক লিখুন। এই লুইস কাঠামোটি চারটি হাইড্রোজেন পরমাণু দ্বারা বেষ্টিত একটি কার্বন পরমাণুর প্রতিনিধিত্ব করে। যখন বৈদ্যুতিনগুলি একটি সমবায় বন্ধন দ্বারা সংযুক্ত থাকে, এর অর্থ হ'ল কার্বন প্রতিটি হাইড্রোজেন পরমাণুর সাথে একটি ইলেকট্রন ভাগ করে এবং এটি হাইড্রোজেনের ক্ষেত্রেও প্রযোজ্য।
- এই উদাহরণের আণবিক সূত্রটি সিএফ 4, মিথেনের।
-
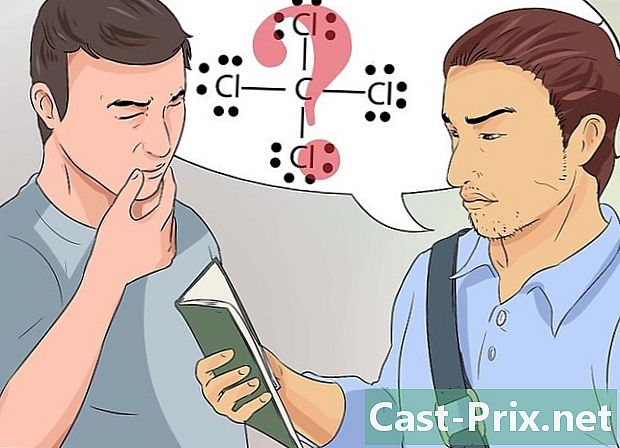
কীভাবে ইলেক্ট্রনগুলি তাদের বন্ড অনুযায়ী সাজানো যায় তা শিখুন। লুইস স্ট্রাকচারগুলি রাসায়নিক বন্ডগুলির একটি সরল দৃষ্টিভঙ্গি উপস্থাপনা।- রাসায়নিক বন্ড এবং লুইস সূত্র সম্পর্কে নির্দিষ্ট ধারণাটি যদি আপনি বুঝতে না পারেন তবে সেগুলি আপনার শিক্ষক বা অধ্যয়ন গোষ্ঠীর সাথে আলোচনা করুন।
-
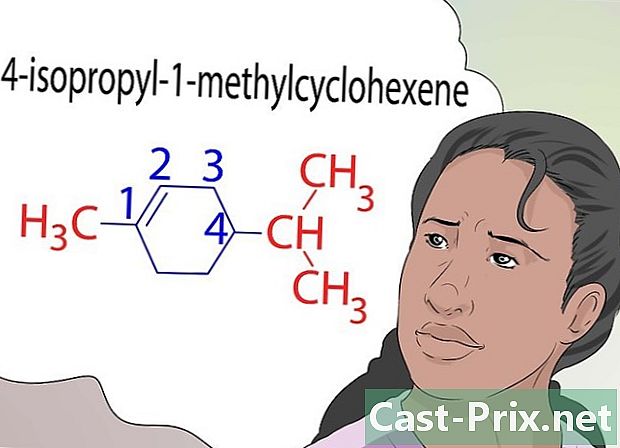
যৌগিক নামকরণ করতে শিখুন। নামকরণ সংক্রান্ত রসায়নের নিজস্ব নিয়ম রয়েছে। কোনও যৌগের সাথে যে ধরণের প্রতিক্রিয়া দেখা দেয়, বাইরের স্তরে বৈদ্যুতিনের ক্ষতি বা সংযোজন এবং যৌগের স্থায়িত্ব বা অস্থিরতা রাসায়নিক উপাদানগুলির নামকরণ সম্ভব করে তোলে। -

রসায়নের নামকরণকে অবমূল্যায়ন করবেন না। বেশিরভাগ ক্ষেত্রে, রসায়নের প্রথম অধ্যায়গুলি নামকরণের উপর দৃষ্টি নিবদ্ধ করে। প্রায়শই, রাসায়নিক যৌগগুলির ভুল পরিচয় আপনাকে পর্যালোচনা করতে ব্যর্থ করতে পারে।- যদি সম্ভব হয় তবে কীভাবে আপনার কোর্স শুরু করার আগে রাসায়নিক যৌগের নামকরণ করবেন তা শিখুন। আপনি একটি গাইড কিনতে বা অনলাইনে সংস্থানগুলির পরামর্শ নিতে পারেন।
-
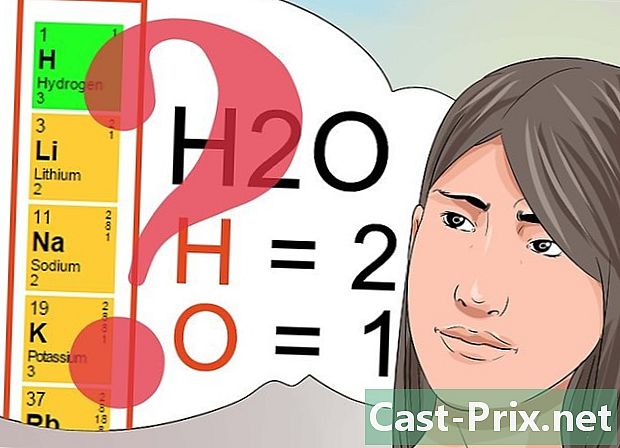
সুপারস্ক্রিপ্ট এবং সাবস্ক্রিপ্টে সংখ্যার অর্থ বুঝুন। আপনি যদি পরীক্ষায় পাস করতে চান তবে এই সংখ্যাগুলির অর্থ কী তা বোঝা গুরুত্বপূর্ণ।- সুপারসক্রিপ্টে রাখা সংখ্যাগুলি একটি প্যাটার্ন অনুসরণ করে যা পর্যায় সারণীতে প্রদর্শিত হয় এবং রাসায়নিক উপাদান বা রাসায়নিক যৌগের মোট চার্জ নির্দেশ করে। পর্যায় সারণীটি পুনরাবৃত্তি করুন এবং আপনি দেখতে পাবেন যে একই উল্লম্ব কলাম (গোষ্ঠী) বরাবর সাজানো উপাদানগুলি একই পরিমাণকে ঘনিষ্টর দ্বারা ভাগ করে।
- রাসায়নিক যৌগের অংশ হিসাবে চিহ্নিত প্রতিটি উপাদানটির পরিমাণ নির্ধারণ করতে ইন্ডেন্টেড নম্বর ব্যবহার করা হয়। উপরে উল্লিখিত হিসাবে, অণু H2O এর সূচক 2 নির্দেশ করে যে দুটি হাইড্রোজেন পরমাণু রয়েছে।
-

পরমাণুগুলি একে অপরের সাথে কীভাবে প্রতিক্রিয়া দেখায় তা আবিষ্কার করুন। রসায়নে ব্যবহৃত নামকরণের অংশের মধ্যে নির্দিষ্ট ধরণের প্রতিক্রিয়া থেকে প্রাপ্ত পণ্যের নামকরণের সুনির্দিষ্ট বিধি অন্তর্ভুক্ত রয়েছে।- এর মধ্যে একটি প্রতিক্রিয়া হ'ল জারণ-হ্রাস-প্রতিক্রিয়া। এটি এমন একটি প্রতিক্রিয়া যার মধ্যে ইলেক্ট্রনগুলি অর্জিত বা হারিয়ে যায়।
- ডক্সিডোরডাকশন প্রতিক্রিয়া চলাকালীন ঘটে যাওয়া প্রক্রিয়াটি মনে রাখার জন্য, নামটি মুখস্থ করুন RROO। এটি মনে রাখার একটি সহজ উপায় অক্সিডেন্ট যখন পায় তখন রিডিউসার ইলেক্ট্রন তৈরি করে.
-
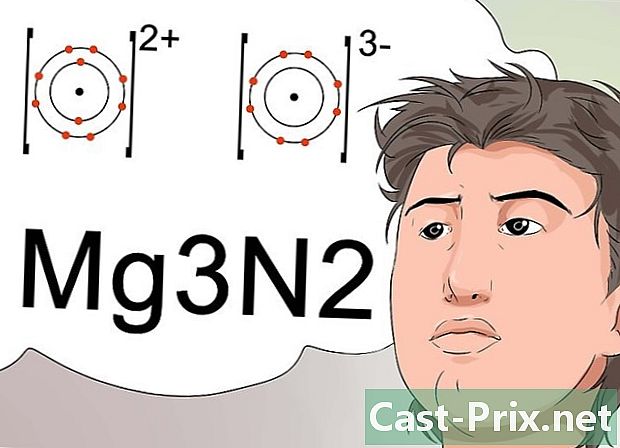
একটি নিরপেক্ষ অণু পেতে সংকেতের সংখ্যাগুলি ব্যবহার করুন। বিজ্ঞানীরা কোনও যৌগের নির্দিষ্ট অণু সূত্রটি সনাক্ত করতে ক্লু ব্যবহার করেন এবং এটিও ইঙ্গিত দেয় যে একটি যৌগ একটি নিরপেক্ষ চার্জের সাথে স্থিতিশীল।- একটি স্থিতিশীল বৈদ্যুতিন কনফিগারেশন এ পৌঁছানোর জন্য, সমান তীব্রতার নেতিবাচক আয়ন (আয়ন) দ্বারা ধনাত্মক আয়ন (কেশন) ক্ষতিপূরণ দিতে হবে। প্রদর্শনকারীরা বোঝা উপস্থাপন।
- উদাহরণস্বরূপ, সিংহ ম্যাগনেসিয়াম +2 এর ইতিবাচক চার্জ বহন করে এবং সিংহ নাইট্রোজেনের -3 এর নেতিবাচক চার্জ রয়েছে। +2 এবং -3 নম্বরগুলি সুপারস্ক্রিপ্টে রাখা উচিত। একটি নিরপেক্ষ অণু পাওয়ার জন্য দুটি উপাদানকে যথাযথভাবে একত্রিত করার জন্য, 2 নাইট্রোজেন পরমাণুর জন্য 3 ম্যাগনেসিয়াম পরমাণু ব্যবহার করা প্রয়োজন।
- প্রাপ্ত অণু সুতরাং এমজি 3 এন 2।
-
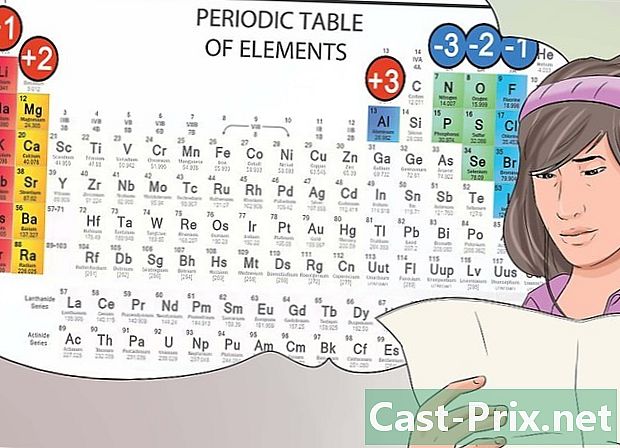
তাদের অবস্থান থেকে অয়নগুলি এবং কেশনগুলি সনাক্ত করুন। পর্যায় সারণীতে প্রথম গোষ্ঠীর অন্তর্ভুক্ত উপাদানগুলিকে ক্ষারীয় ধাতু হিসাবে বিবেচনা করা হয় এবং +1 এর ইতিবাচক চার্জ থাকে। সোডিয়াম (না +) এবং লিথিয়াম (লি +) এর উদাহরণ।- ক্ষারীয় পৃথিবী ধাতুগুলি দ্বিতীয় গ্রুপের অংশ এবং 2+ কেশন তৈরি করে যেমন ম্যাগনেসিয়াম (এমজি 2 +) এবং বেরিয়াম (বা 2+)।
- পর্যায় সারণির সপ্তম কলামের অন্তর্ভুক্ত রাসায়নিক উপাদানগুলি হ্যালোজেনগুলির পরিবার গঠন করে এবং নেতিবাচক চার্জ সহ অয়নগুলি তৈরি করে - যেমন ক্লোরিন (সিএল-) এবং লিওড (আই-)।
-

সর্বাধিক সাধারণ কেশনস এবং অ্যানিয়োনগুলি সনাক্ত করুন। আপনার রসায়ন পরীক্ষায় সাফল্যের জন্য আপনাকে যতটা সম্ভব উপাদানগুলির গ্রুপগুলির নামকরণের পরিমাণ জানতে হবে যার জন্য খাঁজকারীর সংখ্যা পরিবর্তন হয় না।- অন্য কথায়, ম্যাগনেসিয়াম সর্বদা এমজি দ্বারা প্রতিনিধিত্ব করা হয় এবং সর্বদা একটি +2 ধনাত্মক চার্জ থাকে।
-

তথ্য দিয়ে নিজেকে অভিভূত না করার চেষ্টা করুন। বিভিন্ন রাসায়নিক বিক্রিয়া, বৈদ্যুতিন এক্সচেঞ্জ এবং উপাদান বা যৌগের বৈদ্যুতিক চার্জের পরিবর্তন সম্পর্কিত সমস্ত বিস্তৃত তথ্য বোঝা এবং মনে রাখা সহজ নয় not- বর্ণনামূলক পদগুলির সাথে আপনি বুঝতে পারেন না এমন বিষয়গুলি প্রকাশ করুন। উদাহরণস্বরূপ, আপনি যদি জারণ প্রতিক্রিয়া বুঝতে না পারেন বা কীভাবে উপাদানগুলি নেতিবাচক এবং ধনাত্মক চার্জের সাথে সংযুক্ত করে, তাই বলুন। আপনার কাছে সমস্যাযুক্ত ধারণা এবং ধারণাটি স্পষ্টভাবে প্রকাশের মাধ্যমে আপনি লক্ষ্য করতে পারেন যে জিনিসের উপর আপনার অনেক নিয়ন্ত্রণ রয়েছে control
-

নিয়মিত আপনার শিক্ষকের সাথে দেখা করুন। আপনি বুঝতে না পারছেন এমন বিষয়ের একটি তালিকা তৈরি করুন এবং আপনার শিক্ষককে সাহায্যের জন্য জিজ্ঞাসা করুন। আরও জটিল এবং বোধগম্য-বোধগম্য বোঝার জন্য শ্রেণিকক্ষের ধারণাগুলি প্রবেশের আগে জটিল ধারণাগুলিকে একীভূত করার একটি সুযোগ এটি। -

নিজেকে বলুন যে আপনি একটি নতুন ভাষা শিখছেন। চার্জগুলি নির্দেশ করার জন্য লিখিত সূত্রগুলি বুঝতে হবে, একটি রেণুতে সংখ্যা ডেটোম এবং অণুর মধ্যে গঠিত বন্ডগুলি রসায়নের ভাষার অংশ।এটি গ্রাফিক্য উপস্থাপনের এবং রাসায়নিক ক্রিয়াকলাপের সময় সংঘটিত বিভিন্ন রূপান্তরগুলি লেখার একটি উপায় যা আমরা দেখতে পাচ্ছি না।- খালি চোখে যদি সমস্ত প্রক্রিয়াটি পর্যবেক্ষণ করা যায় তবে রসায়ন বোঝা অনেক সহজ হবে। তবে, আপনাকে অবশ্যই ঘটনাকে বর্ণনা করতে রসায়নে ব্যবহৃত পরিভাষা, পাশাপাশি প্রতিক্রিয়াগুলির প্রক্রিয়াগুলি বোঝার চেষ্টা করতে হবে।
- আপনার যদি রসায়ন শ্রেণি বুঝতে সমস্যা হয় তবে জেনে রাখুন যে আপনি একা নন। তবে বোকা বানাবেন না। আপনার শিক্ষকের সাথে কথা বলুন, একটি দলে পড়াশুনা করুন, আপনার শিক্ষকের সহকারীটির সাথে যোগাযোগ করুন বা কেমিস্ট্রিতে সত্যই ভাল এমন কারও কাছ থেকে সহায়তা চাইতে পারেন। আপনি পুরো কোর্সটি শিখতে পারেন তবে সাহায্যের জন্য জিজ্ঞাসা করা ভাল লাগবে যাতে নির্দিষ্ট অধ্যায়গুলি আরও ভালভাবে বোঝার জন্য আমরা আপনাকে এটি ব্যাখ্যা করতে পারি।